Влияние ржавчины на скорость коррозии железа.
«…а машинка-то у вас зацвела, продавать пора» - из разговора маляра с клиентом в автосервисе.
Давайте разберемся, так ли это на самом деле. Как влияет слой ржавчины на поверхности железа на дальнейшее разрушение (коррозию)?
Что такое окисление (коррозия) металла мы уже знаем. Ржавчиной будем называть красно-бурое соединение — гидроксид железа (Fe203H20).
Вспомним школьные уроки химии, попробуем измерить поверхностный потенциал листа низкосортного железа. Подробнее здесь, тут и там.)))
В простейшем варианте способ измерения может быть таким:
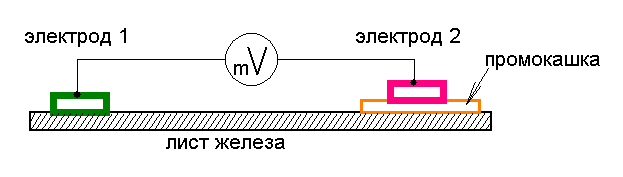
Электрод 1 непосредственно контактирует с листом исследуемого железа. Контактирующие поверхности предварительно очищены от грязи и ржавчины (зашкурены), сухие, плотно прижаты.
Электрод 2 (эталон) касается листа железа через смоченную в электролите (раствор соли) промокашку. Если электрод 2 из химически чистого не окисленного железа (электродный потенциал =-441мВ), то вольтметр покажет нам реальную разницу потенциалов исследуемой поверхности и эталона (чистое железо), т.е. степень «ржавости» + влияние артефактов (инородных вкраплений).
Если использовать в качестве электрода свежезашкуренный кусочек железа от исследуемого образца, то показания вольтметра будут характеризовать только «степень ржавости», т.к. влияние артефактов будет взаимно компенсировано.
Учитывая, что от соприкосновения с электролитом и просто в среде влажного воздуха измерительный (эталонный) электрод 2 будет быстро окисляться, менять свой поверхностный потенциал, лучше использовать для длительных измерений электрод из материала не подверженного окислению с потенциалом=0 (см. ссылки выше).
Именно с таким электродом были получены результаты следующих измерений:

Нижняя половина листа железа сразу после зачистки шкуркой, верхняя – налет ржави от недельного пребывания на улице под навесом при средней влажности 80-90%, апрель 2011г.

Этот лист железа в течение 2-х недель висел на гвоздике за окном, опрыскивался (неравномерно) водопроводной водой 5 раз в сутки.


Фрагмент балки от автомобиля ВАЗ2106, возраст 12 лет.
При небольших усилиях ломается, буквально рассыпается в порошок. Будем считать, что это последняя стадия коррозии металла. Измерить потенциал этого фрагмента не удалось.
Оценим результаты измерений:
Потенциал -360мВ нижней половины верхнего листа будем считать потенциалом совершенно не подвергшегося ржавлению низкосортного железа. Результат -360мВ заметно отличается от -441мВ (для химически чистого железа). Очевидно, сказались примеси в железе и погрешность способа измерения. Но, примем, как есть, т.к. нас интересует не абсолютная величина поверхностного потенциала, а его изменение в зависимости от степени ржавления металла.
Потенциал верхней части того же листа -201мВ, что на 159мВ или в 1,791 раза меньше. Поверхностный потенциал просто катастрофически уменьшается с увеличением ржави. Обратите внимание: потенциал на поверхности толстого слоя ржави в нижней части 2-го листа уже не отрицательный, а положительный +120мВ!!! Это говорит о том, что металл, перешедший в состояние ржавчины, уже не отдает электроны, но жадно стремится их забрать. Откуда он может их забирать? Только из атомов еще целого металла. Т.е. слой ржавчины значительно усиливает скорость коррозии металла.
Таким образом, приходим к выводу, что маляр в автосервисе прав: если машина «зацвела», ее надо срочно продавать. Кому, как не автомаляру знать, насколько трудоемко и практически невозможно расчистить и вывести всю ржавь с кузова автомобиля, включая все скрытые полости, участки сварки, ободрать всю краску с кузова и убедиться, что под слоем краски-грунтовки тоже имеется ржавь…
При использовании УЗ с поверхностными токами (скин-эффектом) можно больше не прислушиваться к советам маляра, убедиться в том, что коррозия остановилась)))
Методы электрохимической защиты увеличивают поверхностный потенциал железа. При использовании катодной защиты с напряжением 12В (напряжение бортовой сети автомобиля) отмечено повышение поверхностного потенциала на 1-2мВ (практически совпадает с погрешностью измерений). Такое незначительное повышение потенциала не приводит к существенному уменьшению скорости коррозии. Но метод защиты с использованием поверхностных токов (скин-эффект) повышает поверхностный потенциал железа минимум на 50-100мВ.